- செயல்பாடு: தானியங்கி, PLC கட்டுப்படுத்தப்பட்டது
- பயன்பாடுகள்: 1,000 Nm³/h H உற்பத்திக்கு2இயற்கை எரிவாயுவிலிருந்து பின்வரும் பயன்பாடுகள் தேவை:
- 380-420 Nm³/h இயற்கை எரிவாயு
- 900 கிலோ/எச் கொதிகலன் ஊட்ட நீர்
- 28 kW மின்சாரம்
- 38 m³/h குளிரூட்டும் நீர் *
- * காற்று குளிரூட்டல் மூலம் மாற்றலாம்
- துணை தயாரிப்பு: தேவைப்பட்டால், நீராவி ஏற்றுமதி
வீடியோ
இயற்கை எரிவாயுவில் இருந்து ஹைட்ரஜன் உற்பத்தி என்பது, அழுத்தப்பட்ட மற்றும் சல்ஃபரைஸ் செய்யப்பட்ட இயற்கை எரிவாயு மற்றும் நீராவியின் இரசாயன எதிர்வினையை ஒரு சிறப்பு சீர்திருத்தத்தில் வினையூக்கியுடன் நிரப்பி H₂, CO₂ மற்றும் CO உடன் சீர்திருத்த வாயுவை உருவாக்கி, சீர்திருத்த வாயுக்களில் CO ஐ CO₂ ஆக மாற்றி பின்னர் பிரித்தெடுக்க வேண்டும். பிரஷர் ஸ்விங் அட்ஸார்ப்ஷன் (PSA) மூலம் சீர்திருத்த வாயுக்களில் இருந்து தகுதி பெற்ற H₂.
ஹைட்ரஜன் உற்பத்தி ஆலை வடிவமைப்பு மற்றும் உபகரணத் தேர்வு விரிவான TCWY பொறியியல் ஆய்வுகள் மற்றும் விற்பனையாளர் மதிப்பீடுகளின் விளைவாகும், குறிப்பாக பின்வருவனவற்றை மேம்படுத்துகிறது:
1. பாதுகாப்பு மற்றும் செயல்பாட்டின் எளிமை
2. நம்பகத்தன்மை
3. குறுகிய உபகரண விநியோகம்
4. குறைந்தபட்ச களப்பணி
5. போட்டி மூலதனம் மற்றும் இயக்க செலவுகள்
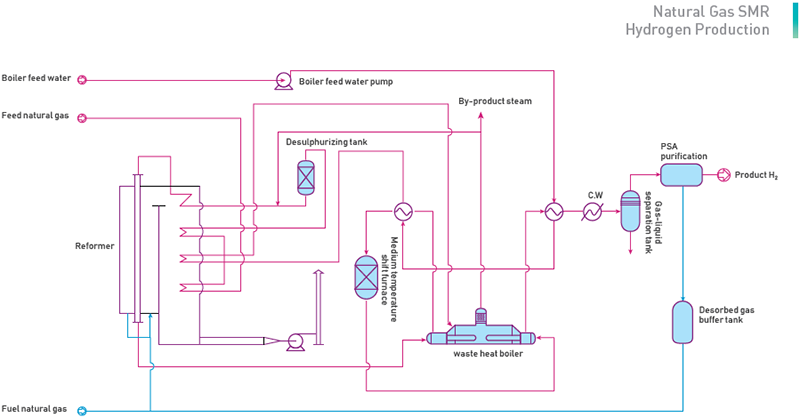
(1) இயற்கை எரிவாயு டீசல்ஃபரைசேஷன்
ஒரு குறிப்பிட்ட வெப்பநிலை மற்றும் அழுத்தத்தில், மாங்கனீசு மற்றும் துத்தநாக ஆக்சைடு உறிஞ்சியின் ஆக்சிஜனேற்றத்தின் மூலம் தீவன வாயுவுடன், நீராவி சீர்திருத்தத்திற்கான வினையூக்கிகளின் தேவைகளைப் பூர்த்தி செய்ய ஊட்ட வாயுவில் உள்ள மொத்த கந்தகம் 0.2ppm க்கு கீழே இருக்கும்.
முக்கிய எதிர்வினை:
| COS+MnO |
| MnS+H2ஓ |
| H2S+ZnO |
(2) NG நீராவி சீர்திருத்தம்
நீராவி சீர்திருத்த செயல்முறை நீராவியை ஆக்ஸிஜனேற்றியாகப் பயன்படுத்துகிறது, மேலும் நிக்கல் வினையூக்கி மூலம், ஹைட்ரோகார்பன்கள் ஹைட்ரஜன் வாயுவை உற்பத்தி செய்வதற்கான மூல வாயுவாக சீர்திருத்தப்படும். இந்த செயல்முறையானது உலையின் கதிர்வீச்சுப் பிரிவில் இருந்து வெப்ப விநியோகத்தைக் கோரும் எண்டோடெர்மிக் செயல்முறையாகும்.
நிக்கல் வினையூக்கிகளின் முன்னிலையில் முக்கிய எதிர்வினை பின்வருமாறு:
| CnHm+nH2O = nCO+(n+m/2)H2 |
| CO+H2O = CO2+H2 △H°298= – 41KJ/mol |
| CO+3H2 = சிஎச்4+H2O △H°298= – 206KJ/mol |
(3) PSA சுத்திகரிப்பு
இரசாயன அலகு செயல்முறையாக, PSA வாயு பிரிப்பு தொழில்நுட்பம் ஒரு சுயாதீனமான ஒழுக்கமாக வேகமாக வளர்ந்து வருகிறது, மேலும் பெட்ரோகெமிக்கல், ரசாயனம், உலோகம், மின்னணுவியல், தேசிய பாதுகாப்பு, மருத்துவம், ஒளி தொழில், விவசாயம் மற்றும் சுற்றுச்சூழல் பாதுகாப்பு ஆகிய துறைகளில் மேலும் மேலும் பரவலாகப் பயன்படுத்தப்படுகிறது. தொழில்கள், முதலியன. தற்போது, PSA ஆனது H இன் முக்கிய செயல்முறையாக மாறியுள்ளது2கார்பன் டை ஆக்சைடு, கார்பன் மோனாக்சைடு, நைட்ரஜன், ஆக்ஸிஜன், மீத்தேன் மற்றும் பிற தொழில்துறை வாயுக்களின் சுத்திகரிப்பு மற்றும் பிரிப்புக்கு வெற்றிகரமாகப் பயன்படுத்தப்பட்ட பிரிப்பு.
நல்ல நுண்துளை அமைப்பைக் கொண்ட சில திடப் பொருட்கள் திரவ மூலக்கூறுகளை உறிஞ்சும் என்றும், அத்தகைய உறிஞ்சக்கூடிய பொருள் உறிஞ்சக்கூடியது என்றும் ஆய்வில் கண்டறியப்பட்டுள்ளது. திரவ மூலக்கூறுகள் திட உறிஞ்சிகளைத் தொடர்பு கொள்ளும்போது, உறிஞ்சுதல் உடனடியாக நிகழ்கிறது. உறிஞ்சுதல் திரவம் மற்றும் உறிஞ்சக்கூடிய மேற்பரப்பில் உறிஞ்சப்பட்ட மூலக்கூறுகளின் வெவ்வேறு செறிவுகளில் விளைகிறது. மற்றும் உறிஞ்சும் மூலம் உறிஞ்சப்பட்ட மூலக்கூறுகள் அதன் மேற்பரப்பில் செறிவூட்டப்படும். வழக்கம் போல், வெவ்வேறு மூலக்கூறுகள் உறிஞ்சிகளால் உறிஞ்சப்படும் போது வெவ்வேறு குணாதிசயங்களைக் காண்பிக்கும். திரவ வெப்பநிலை மற்றும் செறிவு (அழுத்தம்) போன்ற வெளிப்புற நிலைமைகளும் இதை நேரடியாக பாதிக்கும். எனவே, இந்த வகையான வெவ்வேறு குணாதிசயங்களால், வெப்பநிலை அல்லது அழுத்தத்தின் மாற்றத்தால், கலவையின் பிரிப்பு மற்றும் சுத்திகரிப்பு ஆகியவற்றை நாம் அடைய முடியும்.
இந்த ஆலைக்கு, உறிஞ்சும் படுக்கையில் பல்வேறு உறிஞ்சிகள் நிரப்பப்படுகின்றன. சீர்திருத்த வாயு (எரிவாயு கலவை) ஒரு குறிப்பிட்ட அழுத்தத்தின் கீழ் உறிஞ்சுதல் நெடுவரிசையில் (உறிஞ்சும் படுக்கை) பாயும் போது, H இன் வெவ்வேறு உறிஞ்சுதல் பண்புகள் காரணமாக2, CO, CH2, CO2, முதலியன CO, CH2மற்றும் CO2உறிஞ்சிகளால் உறிஞ்சப்படுகிறது, அதே நேரத்தில் எச்2தகுதியான தயாரிப்பு ஹைட்ரஜனைப் பெற படுக்கையின் மேல் இருந்து வெளியேறும்.










 MnS+CO2
MnS+CO2









